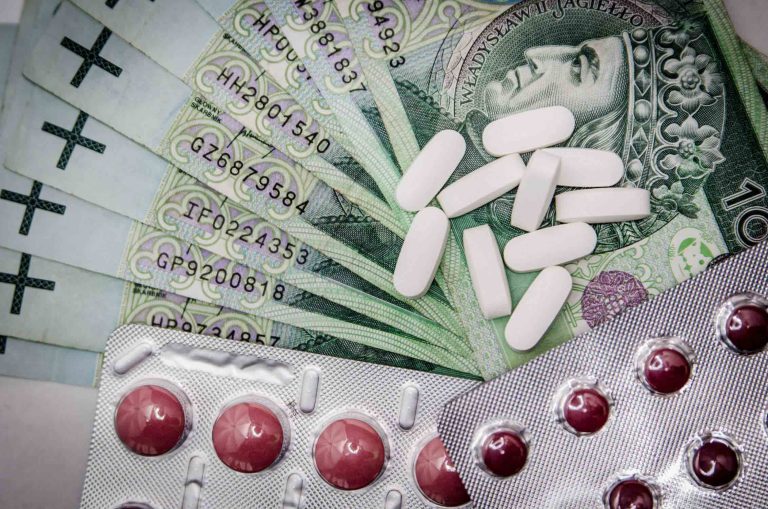
venetoclax适用治疗的漫性淋巴细胞白血病与不易治或反复性缺失17p突变基因的患者。
venetoclax(维奈托克)是第一个靶向治疗B细胞淋巴瘤因素2(BCL-2)的可选择性抑制药。由美国罗氏制药企业(Abb Vie Inc)和德国瑞士罗氏公司(Roche Group)集团旗下的基因泰克(Genentech)企业合作研发。于2016年4月11日批准发售,适用治疗的漫性淋巴细胞白血病与不易治或反复性缺失17p突变基因的患者。2018年6月8日,美国食品和药物管理局(FDA)准许venetoclax(VENCLEXTA,AbbVie Inc.和Genentech Inc.)治疗漫性淋巴细胞白血病(CLL)或小淋巴细胞淋巴肿瘤(SLL)患者,不管有没有17p缺失,但是至少接纳过一次治疗。2019年5月15日,FDA准许了venetoclax与奥比妥珠单抗的搭配治疗法,用以一线CLL/SLL治疗。
漫性淋巴细胞白血病(CLL)是最常见的成年人白血病之一 。 患者细胞中的B细胞淋巴瘤因素(BCL-2)能促进肿瘤细胞生长发育 , 在漫性淋巴细胞白血病和其它B体细胞肿瘤中常会过多表述 。 新诊断的病案中 , 约10%患者归属于性染色体17p缺失型 , 发作型病案中这一比率达到20% 。 性染色体17p能够抑制癌细胞生长发育 , 当性染色体17p缺失时 , CLL患者一般均值存活期不得超过3年 。 而venetoclax(维奈托克)恰好是该类病症的动画特效靶向治疗药物!
AbbVie 副书记兼首席总裁Michael Severino博士说:“此项FDA的准许为患者提供了一种新的无放化疗协同治疗计划方案,并强调了venetoclax(维奈托克)将会越来越多的用于漫性淋巴细胞白血病(CLL)的治疗中。该核准的依据是患者得到了12月治疗的CLL14试验的结论。在本实验操作中,接纳venetoclax(维奈托克)的大部分患者在两年内维持无进度。”